塩化銀(I)
塩化銀(I)(えんかぎん いち、英: silver(I) chloride)は、化学式が AgCl と表される銀の塩化物である。通常、単に「塩化銀」と言った場合はこの塩化銀(I)を指す。天然には角銀鉱という鉱物として産する。
| 塩化銀(I) | |
|---|---|
 | |
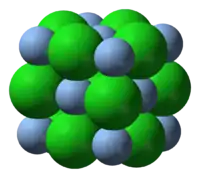 | |
silver(I) chloride | |
別称 塩化銀 | |
| 識別情報 | |
| CAS登録番号 | 7783-90-6 |
| 特性 | |
| 化学式 | AgCl |
| モル質量 | 143.321 g mol−1 |
| 外観 | 無色結晶 |
| 密度 | 5.56 g cm−3, 固体 |
| 融点 |
455 °C, 728 K, 851 °F |
| 沸点 |
1550 °C, 1823 K, 2822 °F (分解) |
| 水への溶解度 | 0.00008 g/100 cm3 (10 °C) |
| 構造 | |
| 結晶構造 | 立方晶系 |
| 熱化学 | |
| 標準生成熱 ΔfH |
−127.068 kJ mol−1[1] |
| 標準モルエントロピー S |
96.2 J mol−1K−1 |
| 標準定圧モル比熱, Cp |
50.79 J mol−1K−1 |
| 危険性 | |
| NFPA 704 |
 0
2
0
|
| 関連する物質 | |
| 関連物質 | フッ化銀(I) 臭化銀(I) ヨウ化銀(I) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
性質
水溶液中ではほとんど電離せず弱電解質[2]・難溶性であるため、沈殿する。塩化物イオンの銀(I)イオンに対する錯生成定数は 103.04 である[3]。溶解度積は以下の通りである[4]。
配位子となるイオンや分子が存在すれば溶解する。チオ硫酸イオン、シアン化物イオン、アンモニアによってそれぞれ
となって溶解することは広く知られているが、濃食塩水や塩酸にも錯イオンを作って溶解する。
また、濃厚な硝酸銀(I)あるいは過塩素酸銀(I)などの銀塩水溶液に対しても幾分溶解度が増大し、以下のような錯イオンを生成することが知られている[2]。
感光性があり光によって容易に分解し、紫色を経て黒変する。
塩化銀(I)の白色沈殿をるつぼに入れて加熱すると455 °Cで融解する。その融解液を冷却すると固体になるが、イオン結晶でありながら塑性変形する。また、電気伝導性があることが知られている。Ag-Cl 結合はある程度の共有結合性を帯びる。
結晶構造
結晶は塩化ナトリウム型構造であり、その格子定数はa = 5.54 Å、Ag-Cl 結合距離は2.77 Åである[5]。
脚注
- D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem. Ref. Data 11 Suppl. 2 (1982).
- F.A. コットン, G. ウィルキンソン著, 中原 勝儼訳 『コットン・ウィルキンソン無機化学』 培風館、1987年
- 日本化学会編 『化学便覧 基礎編 改訂4版』 丸善、1993年
- 新良宏一、庄野利之 益田勲 共訳 『基礎分析化学』 三共出版、1982年
- 『化学大辞典』 共立出版、1993年
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.