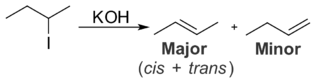ザイツェフ則
有機化学において、ザイツェフ則(ザイツェフそく、英語: Zaitsev's rule、ザイチェフ則や英語読みのセイチェフ則とも)は、脱離反応において多く生成するアルケンを予測するための経験則である。ロシアの化学者アレクサンドル・ザイツェフはカザン大学にいたときにさまざまな脱離反応を研究し、結果生じるアルケンの一般的な傾向を観察した。この傾向に基づいてザイツェフは「最も多く生成されたアルケンは、水素置換基が最も少ないα炭素から水素を取り除くことに対応する」と述べた。例えば、2-ヨードブタンをアルコール性の水酸化カリウム(KOH)で処理すると、2-ブテンが主生成物となり、1-ブテンが副生成物となる[1]。
より一般的には、ザイツェフ則は脱離反応において最も置換された生成物が最も安定であり、それゆえ最も多く生じると予測している。この法則は新たに形成されたアルケンの立体化学については一般化を行うことができず、脱離反応の位置化学のみについて説明する。多くの脱離反応で多く生成する生成物を予測するのに有効であるが、多くの例外がある。
歴史

アレクサンドル・ザイツェフは1875年にJustus Liebigs Annalen der Chemieで脱離反応の生成物に関して観察した結果を初めて発表した[2][3]。この論文にはザイツェフの学生が行った独自の研究が含まれているが、主に文献のレビューであり、それ以前に発表された研究に大きく依存していた[4]。この中でザイツェフはヨウ化アルキルの脱ハロゲン化水素において多く生じる位置化学を予測するための単に経験的な法則を提案した。この法則は他のさまざまな脱離反応にも適用できることが分かった。ザイツェフの論文は20世紀を通してよく参照されたが、教科書で「ザイツェフ則」という用語が使われ始めたのは1960年代になってからであった[3]。
この法則を最初に発表したのはザイツェフではない。アレクサンドル・ニコラエヴィチ・ポポフが1872年にザイツェフ則と似た経験則を発表し[5]、この発見を1873年にカザン大学で発表している。ザイツェフは以前の研究でポポフの1872年の論文を引用し、またカザン大学にいたためポポフが提案した法則をおそらく知っていたが、ザイツェフが1875年にLiebigs Annalenで発表した論文ではポポフの研究には言及されていない[3][4]。
ザイツェフ則に関する議論は、ウラジーミル・マルコフニコフに言及せずには不完全であろう。ザイツェフとマルコフニコフはともにアレクサンドル・ブートレロフの下で研究し、同じ時期にカザン大学で教鞭をとり激しいライバル関係にあった。ザイツェフと現在マルコフニコフ則として知られる法則を1870年に発表したマルコフニコフは脱離反応に関して相反する見解を持った。マルコフニコフは最も置換されていないアルケンが最も多く生じると考えたが、ザイツェフは最も置換されたアルケンが主生成物であると考えた。おそらくザイツェフが脱離反応の研究を始めた主な理由の1つはライバルを反証することであった[3]。マルコフニコフがComptes Rendusで付加反応の法則を細かく説明する3部構成のarticleの最初を発表した直後に、ザイツェフが脱離反応の法則を発表した[4]。
熱力学的考察
アルケンからアルカンへの水素化は発熱的である。水素化反応中に放出されるエネルギー量(水素化熱として知られる)は、最初のアルケンの安定性に反比例する。アルケンが安定であればあるほど水素化熱は低くなる。さまざまなアルケンの水素化熱を調べると、置換量とともに安定性が向上することが分かる[6]。
| 化合物の名前 | 構造 | 水素化のモル熱 | 置換度 | |
|---|---|---|---|---|
| kJ/mol | kcal/mol | |||
| エチレン | 137 | 32.8 | 置換されていない | |
| 1-ブテン | 127 | 30.3 | 一置換 | |
| トランス-2-ブテン | 116 | 27.6 | 二置換 | |
| 2-メチル-2-ブテン | 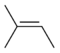 |
113 | 26.9 | 三置換 |
| 2,3-ジメチル-2-ブテン |  |
111 | 26.6 | 四置換 |
置換基を加えることに関連する安定性の増加は、いくつかの要因の結果である。アルキル基は誘導効果による電子供与であり、アルケンのσ結合の電子密度を増加させる。さらに、アルキル基は立体的に大きく、互いに離れていると最も安定する。アルカンでは、最大の分離は四面体結合角109.5°である。アルケンでは結合角は120°近くまで大きくなる。結果として、アルキル基の間の分離は最も置換されたアルケンで最大になる[7]。
アルキル基のHOMOと二重結合のLUMOの間の安定化相互作用を説明する超共役も、アルケンの安定に対するアルキル置換の影響を説明するのに役立つ。軌道混成において、sp2炭素とsp3炭素間の結合は2つのsp3混成炭素間の結合よりも強い。計算により、アルキル基1つあたり6 kcal/molの支配的な安定化超共役効果が分かっている[8]。
立体効果
E2反応において、塩基はハロゲン化物などの脱離基に対してβであるプロトンを引き抜く。プロトンの除去と脱離基の除去は新たな二重結合を形成する単一の協調した段階で生じる。水酸化ナトリウム、ナトリウムメトキシド、ナトリウムエトキシドなどの小さく妨げられていない塩基をE2脱離に使用する場合、普通、ザイツェフ生成物がホフマン生成物として知られる最も置換されていないアルケンよりも好まれる。例えば、2-ブロモ-2-メチルブタンをエタノール中でナトリウムエトキシドで処理すると、適度な選択性でザイツェフ生成物が生成される[9]。
立体相互作用により、カリウム t-ブトキシド、トリエチルアミン、2,6-ルチジンなどのかさ高い塩基は、ザイツェフ生成物になるようにプロトンを容易に引き抜くことができない。これらの状況では、立体障害の少ないプロトンが優先的に引き抜かれる。結果としてかさ高い塩基を使用するときはホフマン生成物が多く生じる。2-ブロモ-2-メチルブタンをナトリウムエトキシドではなくカリウム t-ブトキシドで処理すると、ホフマン生成物が多く生成される[10]。
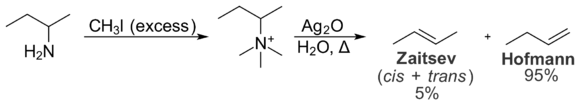
基質内の立体相互作用もザイツェフ生成物の形成を妨げる。これらの分子内相互作用は、アミンをアルケンに変換するホフマン脱離反応における生成物の分布に関連する。ホフマン脱離において、第四級ヨウ化アンモニウム塩を酸化銀で処理すると、水酸化物イオンが生成され、これは塩基として働き第三級アミンを除去してアルケンを生成する[11]。
ホフマン脱離においては、分子内の立体相互作用により最も置換されていないアルケンが一般的に多く生成される。第四級アンモニウム基は大きく、分子の残りの部分のアルキル基との相互作用は望ましくない。結果として、ザイツェフ生成物の形成に必要な立体配座は、ホフマン生成物の形成に必要な立体配座よりもエネルギー的に有利でない。その結果、ホフマン生成物がより多く形成される。コープ脱離は原理的にはホフマン脱離と非常に似ているが、より穏やかな条件下で生じる。これはホフマン脱離を同じ理由でホフマン生成物の形成を支持する[12]。
立体化学
場合によっては、出発物質の立体化学がザイツェフ生成物の形成を妨げることがある。例えば、塩化メンチルをナトリウムエトキシドで処理すると、ホフマン生成物が専ら生成される[13]。ただし収率は非常に低い[14]。
この結果は出発物質の立体化学によるものである。E2脱離にはアンチペリプラナー幾何学が必要である。この場合プトロンと脱離基地はC-C結合の反対側にあるが、同じ平面上にある。塩化メンチルがいす形の立体配座で描かれるとき、異常な生成物分布を説明するのは簡単である。
ザイチェフ生成物を生成するには2位での脱離が必要であるが、イソプロピル基(プロトンではない)は塩素脱離基に対してアンチペリプラナーである。これにより2位での脱離が不可能になる。ホフマン生成物が生成されるためには、6位で脱離が行われなければならない。この位置でのプロトンは脱離基に対して正しい方向を向いているため、脱離が生じる可能性がある。結果としてこの特定の反応はホフマン生成物のみを生成する。
出典
- Lehman, John (2009). Operational Organic Chemistry (4th ed.). Upper Saddle River, NJ: Pearson Education. p. 182. ISBN 978-0136000921
- Saytzeff, Alexander (1875). “Zur Kenntniss der Reihenfolge der Analgerung und Ausscheidung der Jodwasserstoffelemente in organischen Verbindungen”. Justus Liebigs Annalen der Chemie 179 (3): 296–301. doi:10.1002/jlac.18751790304.
- Lewis, D. E. (1995). “Alexander Mikhailovich Zaytsev (1841–1910) Markovnikov's Conservative Contemporary”. Bulletin for the History of Chemistry 17: 21–30 (27).
- Lewis, D. E. (2010). “Feuding Rule Makers: Aleksandr Mikhailovich Zaitsev (1841–1910) and Vladimir Vasil'evich Markovnikov (1838–1904). A Commentary on the Origins of Zaitsev's Rule”. Bulletin for the History of Chemistry 35 (2): 115–124 (121–122).
- Popoff, Aleksandr (1872). “Die Oxydation der Ketone als Mittel zur Bestimmung der Constitution der fetten Säuren und der Alkohole”. Justus Liebigs Annalen der Chemie 162 (1): 151–160. doi:10.1002/jlac.18721620112.
- Wade, pp. 292–294.
- Wade, p. 293.
- The Physical Origin of Saytzeff's Rule Benoit Braida, Vinca Prana, and Philippe C. Hiberty Angew. Chem. Int. Ed. 2009, 48, 5724 –5728 doi:10.1002/anie.200901923
- Wade, p. 301.
- Wade, p. 302.
- Wade, pp. 898–901.
- Wade, p. 903.
- Lehman 2009, pp. 183–184
- Hückel, Walter; Tappe, Werner; Legutke, Günter (1940). “Abspaltungsreaktionen und ihr sterischer Verlauf”. Justus Liebig's Annalen der Chemie 543: 191–230. doi:10.1002/jlac.19405430117.
文献
- Wade, L. G. (2010). Organic Chemistry (7th ed.). Upper Saddle River, NJ: Pearson Education. ISBN 978-0321592316
外部リンク
- Online course of chemistry
- English Translation of 1875 German article on 'The order of addition and of elimination of hydrogen and iodine in organic compounds' by Alexander Zaitsev.